పీరియాడిక్ టేబుల్ను NCERT సిలబస్ నుంచి తొలగించడం విద్యార్థులకు నష్టం
ప్రపంచవ్యాప్తంగా మూడు లక్షల యాభై వేల రసాయన సంయోగ పదార్థాలు ఉన్నాయి. ఇవి 118 మూలకాల చేత తయారైనవి. ఈ మూలకాలు రకరకాల నిష్పత్తుల్లో, రకరకాల కలయికలతో రసాయన చర్యలో పాల్గొని తయారైనవే. మన కంటికి కనపడే ప్రతి వస్తువు, మనం తాకే ప్రతి వస్తువు ,మనం తినే తిండి మనం పీల్చే, గాలి మనభూమి సముద్రాలు, ఆకాశంలోని సూర్యచంద్రులు నక్షత్రాలు సమస్తం ఈ 118 మూలకాలు వాటితో తయారైన సంయోగ పదార్థాలతో రూపొందినవే. వీటన్నిటి గురించి తెలుసుకోవడం చాలా కష్టం. అయినా ఒకే ఒక్క పేజీలో ఇమిడే పీరియాడిక్ టేబుల్ ద్వారా చాలా సులభంగా పదార్థ విజ్ఞానం గురించి నేర్చుకోవచ్చు. ఈ పీరియాడిక్ టేబుల్ లో పదార్థాలన్నిటి గురించిన సమగ్రమైన విజ్ఞానం ఉంటుంది. పిరియాడిక్ టేబుల్ను అర్థం చేసుకుంటే సమస్త విశ్వంలోనే లక్షోపలక్షల పదార్థాల గురించి తెలుసుకున్నట్లు. అంతటి ప్రాముఖ్యం గల పీరియాడిక్ టేబుల్ను NCERT సిలబస్ నుంచి ఉన్నత పాఠశాల స్థాయిలో తొలగించడం విద్యార్థుల భవిష్యత్తుకు నష్టం.
పిరియాడిక్ టేబుల్ అంటే మూలకాలను వాటి భౌతిక రసాయన ధర్మాల ఆధారంగా వర్గీకరించడం అంటే మూలకాలను అడ్డు వరుసల్లో( పీరియడ్లు) నిలువరుసల్లో (గ్రూపులు )గా అమర్చడమే .అలా చేయడం వల్ల మూలకాలను , సంయోగ పదార్థాలను గురించి వాటి ధర్మాలను సులభంగా అర్థం చేసుకొని గుర్తుపెట్టుకోవచ్చు. భవిష్యత్తులో రసాయన శాస్త్రాన్ని అభ్యసించే వారికి ఇది పునాది లాగా పనికొస్తుంది. ఒకవేళ పదవ తరగతి లోనే విద్యార్థులు చదువు ఆపివేస్తే పదార్థాల గురించిన ప్రాథమిక అవగాహన విద్యార్థుల్లో ఉంటుంది. ఇప్పుడు ఉన్నత పాఠశాల స్థాయిలో తొలగిస్తే విద్యార్థులకు నష్టం
చరిత్రలో రసాయన శాస్త్రం
మెస్పటోమియా, ఈజిప్టు ,చైనా భారత దేశాల ప్రాచీన నాగరికతలలో రసాయన శాస్త్రపు మూలాలు ఉన్నాయి. ఆ కాలంలో లోహ సంగ్రహణం,కుండల తయారీ, అద్దకం సాంకేతికత అభివృద్ధి అయినాయి.
రసవాదం (Alchemy) క్రీస్తుపూర్వం 300 నుండి క్రీస్తుశకం 1600 వరకు
ఇది ఒక ప్రాచీన సంప్రదాయం ఇది యూరప్, ఆఫ్రికా ,ఆసియాల్లో ప్రాచుర్యంలో ఉండేది. అయితే ఈ రసవాదం శాస్త్రీయ సూత్రాల మీద ఆధారపడి లేదు కానీ ఆధునిక రసాయన శాస్త్రానికి అవసరమైన ప్రయోగశాల సాంకేతికలను పరికరాలను పరిచయం చేసింది.
రసాయన శాస్త్రంలో విప్లవం క్రీస్తు శకం 1600 నుండి 1700 వరకు
రాబర్ట్ బాయిల్ : ఈయన సూక్ష్మ కణ సిద్ధాంతాన్ని( corpuscularion theory) ప్రతిపాదించాడు . ఈ సిద్ధాంతం ప్రకారం పదార్థాల ధర్మాలు, సూక్ష్మ కణాలు విభిన్న కలయికల, ఘర్షణల వలన ఏర్పడతాయి అని అన్నాడు. ఈ సూక్ష్మకణాల చర్యల ద్వారా ద్రావణీయత వంటి రసాయన లక్షణాలు వివరించ బడుతాయని అన్నాడు.
ద్రవ్య నిత్యత్వ నియమం
ఆధునిక రసాయన శాస్త్ర పితామహుడు అయిన ఆంటోనీ లేవోయిజర్ బంధించిన వ్యవస్థలో పదార్థము నశించదు, సృష్టించబడదు అని చెప్పాడు. దీన్ని ద్రవ్య నిత్యత్వ నియమం అంటారు .ఒక రసాయన చర్యలో చర్యకు ముందు చర్యలో పాల్గొనే రసాయన పదార్థాల మొత్తం ద్రవ్యరాశి ఎంతో, రసాయన చర్య తర్వాత ఏర్పడిన రసాయన పదార్థాల ద్రవ్యరాశి మొత్తం అంతే ఉంటుంది మారదు. దీన్నే ద్రవ్య నిత్యత్వ నియమం అంటారు
19వ శతాబ్దంలో డాల్టన్ పరమాణు సిద్ధాంతం అభివృద్ధి అయింది .అలాగే మెండలియేవ్ పీరియాడిక్ టేబుల్ అభివృద్ధి చెందింది. కొత్త మూలకాలు, సంయోగ పదార్థాలు కనుగొనబడ్డాయి. రసాయన శాస్త్రం కీలక మలుపు తిరిగింది. ఫలితంగా 20వ శతాబ్దంలో రసాయన శాస్త్రం అభివృద్ధి వేగం పెంచుకుంది సేంద్రియ రసాయన శాస్త్రం, జీవ రసాయన శాస్త్రం, భౌతిక రసాయన శాస్త్రం వంటి అనేక రసాయన శాస్త్రాలు అభివృద్ధి చెందాయి. మందుల పరిశ్రమల రంగంలోనూ శక్తి ఉత్పాదక రంగాల్లోనూ ప్రగతి సాధ్యమైంది.
రసాయన శాస్త్ర రసాయన శాస్త్ర ప్రగతిని మూలకాల వర్గీకరణ మలుపు తిప్పినది. అందులో భాగంగా డొబరైనర్ సిద్ధాంతం, న్యూ ల్యాండ్ అష్టక సిద్ధాంతం, మెండలీవు పీరియాడిక్ టేబుల్, ఆధునిక పీరియడ్ టేబుల్ ఆవిష్కరణలు చాలా కీలకమైనవి.
ఇంతకీ మనం ఎందుకు మూలకాలను వర్గీకరించాలి?
భవన నిర్మాణానికి ఇటుక రాళ్లు ఎంత ముఖ్యమో అన్ని రకాల పదార్థాల నిర్మాణానికి మూలకాలు అంత ముఖ్యం. వాటి యొక్క భౌతిక రసాయన ధర్మాల మధ్య ఉండే పోలికలు, భేదాలను గుర్తించడం ముఖ్యం. వాటిని గుర్తు పెట్టుకొని , అవగాహన చేసుకుని వినియోగించుకోవడం చాలా ముఖ్యం. అందుకనే మూలకాలను వర్గీకరించాల్సిన అవసరం ఏర్పడింది.
1800 సంవత్సరం వరకు 31 మూలకాలను కనుగొన్నారు. అదే 1865వ సంవత్సరానికి 65 మూలకాలు అంటే రెండింతల మూలకాలను కనుగొన్నారు. ఇప్పుడు 118 మూలకాలు ఉన్నాయి. ఇంకా శాస్త్రవేత్తలు నూతన మూలకాలను కనుగొనే ప్రయత్నంలో ఉన్నారు. కొత్త వాటిని తయారు చేసే ప్రయత్నంలోనూ ఉన్నారు. ఇన్ని మూలకాలు వాటితో ఏర్పడ్డ సంయోగపదార్థాల భౌతిక రసాయన ధర్మాలను విడివిడిగా అధ్యయనం చేయడం కష్టం. ఈ కష్టం నుండి బయటపడి సులభతరం చేయడానికి మూలకాలను వర్గీకరించారు. వాటి రసాయన వాస్తవాలను వెలికి తీయడమే గాక నూతన మూలకాలను కనుగొనడానికీ ఉన్న వాటి గురించి మరింత లోతుగా అధ్యయనం చేయడానికీ మూలకాల వర్గీకరణ ఉపయోగపడుతుంది.
ఆవర్తన పట్టిక (periodic table) పుట్టుక మరియు దాని పరిణామం
మూలకాలను గ్రూపులుగా వర్గీకరించడం, ఆవర్తన నియమాన్ని ఆవర్తన పట్టికను, అభివృద్ధి చేయడం లో అనేక మంది శాస్త్రవేత్తల కృషి ఉంది.
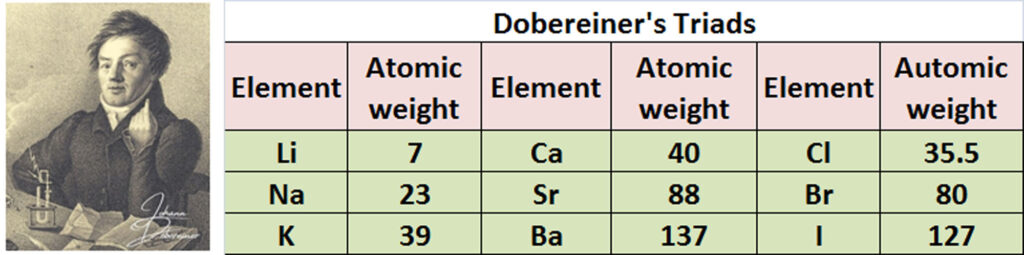
మొట్టమొదట జోహాన్ డొబరైనర్ మూలకాల ధర్మాల పోకడలను గుర్తించాలని 1800 సంవత్సరంలో భావించాడు. 1829లో మూలకాల భౌతిక రసాయన ధర్మాల పోలికలను బట్టి మూడు మూలకాలు గల గ్రూపులను రూపొందించాడు. వీటిని డొబరైనర్ త్రికాలు( Dobariner triats) అని అన్నారు. ప్రతి త్రికంలో మధ్యమూలకపు పరమాణు భారం చివరి రెండింటి యొక్క పరమాణు భారాల సగటుకు సమానంగా ఉంటుంది. చివరి రెండింటి ధర్మాలకు, మధ్య మూలకం ధర్మాలు మధ్యస్థంగా ఉంటాయి దీన్నే డొబరైనర్ త్రిక సిద్ధాంతమంటారు.
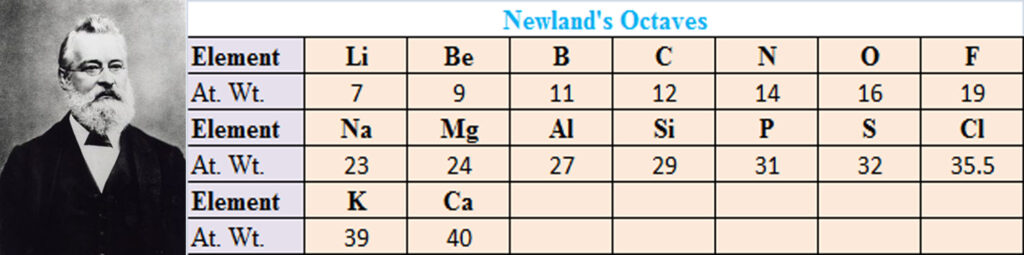
ఆంగ్ల శాస్త్రవేత్త జాన్ అలెగ్జాండర్ న్యూ లాండ్స్ 1965లో అష్టక సిద్ధాంతాన్ని ప్రతిపాదించాడు. ఈయన మూలకాలను పరమాణుభారాల ఆరోహణ క్రమంలో అమర్చాడు. ప్రతి ఎనిమిదవ మూలకం యొక్క ధర్మాలు మొదటి మూలిక ధర్మాలతో పోలి ఉంటుంది. ఇది సంగీతంలోనే సప్త స్వరాలను పోలి ఉంటుంది సంగీతంలో ప్రతి ఎనిమిదవ స్వరం మొదటి స్వరంతో పోలి ఉంటుంది
మనకు నేడు తెలిసిన ఆవర్తన నియమాన్ని (periodic law) డిమెట్రీ మెండలీవ్ ప్రతిపాదించాడు.

మెండలీవ్ మూలకాలను అడ్డు వరుసల్లో, నిలువ వరుసల్లో, వాటి పరమాణు భారాల ఆరోహణ క్రమంలో అమర్చాడు. అలా అమర్చడంలో ధర్మాల్లో పోలికలు ఉండే మూలకాలను నిలువ వరుసల్లో అంటే గ్రూపులుగా అమర్చాడు. అప్పుడు ఒక ప్రధాన విషయం అవగాహనకు వచ్చింది ఏమిటనగా ధర్మాలలో పోలికలు గల మూలకాలు నియమిత వ్యవధిలో మరలా మరలా వస్తున్నాయి .అలా వచ్చి ఒకదాని కింద ఒకటి చేరి గ్రూపులుగా రూపొందుతున్నాయి. దీన్నే మూలకాల ఆవర్తనము చెందడం (re occuring of similar elements) అంటారు. మెండలీవ్ ఆవర్తన నియమపు సారాంశం “మూలకాలను వాటి పరమాణు భారాల ఆరోహణ క్రమంలో అమర్చినప్పుడు వాటి భౌతిక రసాయన ధర్మాలు పరమాణుభారాల ఆవర్తన ప్రమేయాలు”.
మెండలీవ్ ఈ ఆవర్తన నియమం ఆధారంగా పట్టిక తయారు చేశాడు అలా తయారు చేసేటప్పుడు అల్యూమినియం కింద ఖాళీ వదిలాడు అక్కడ “ఎకా అల్యూమినియం” అనే మూలకం ఉండాలని చెప్పాడు. అది అప్పటికి ఇంకా కనుగొనబడ లేదు.
అలాగే సిలికాన్ కింద ఎకాసిలికాన్ అనే మూలకం ఉండాలని కూడా చెప్పాడు. అది కూడా అప్పటికింకా కనుగొనబడలేదు. తర్వాత గేలీలియం ( ఏక అల్యూమినియం)ను జర్మేనియం (ఎకా సిలికాన్ ) కనుగొన్నారు. వీటి ధర్మాలను మెండలీవు ముందే చెప్పాడు. అప్పటినుండి మెండలీవు పీరియాడిక్ టేబుల్ ప్రాచుర్యంలోకి వచ్చింది. 1905లో ఈ పీరియాడిక్ టేబుల్ ని మెండలీవు ప్రచురించాడు.
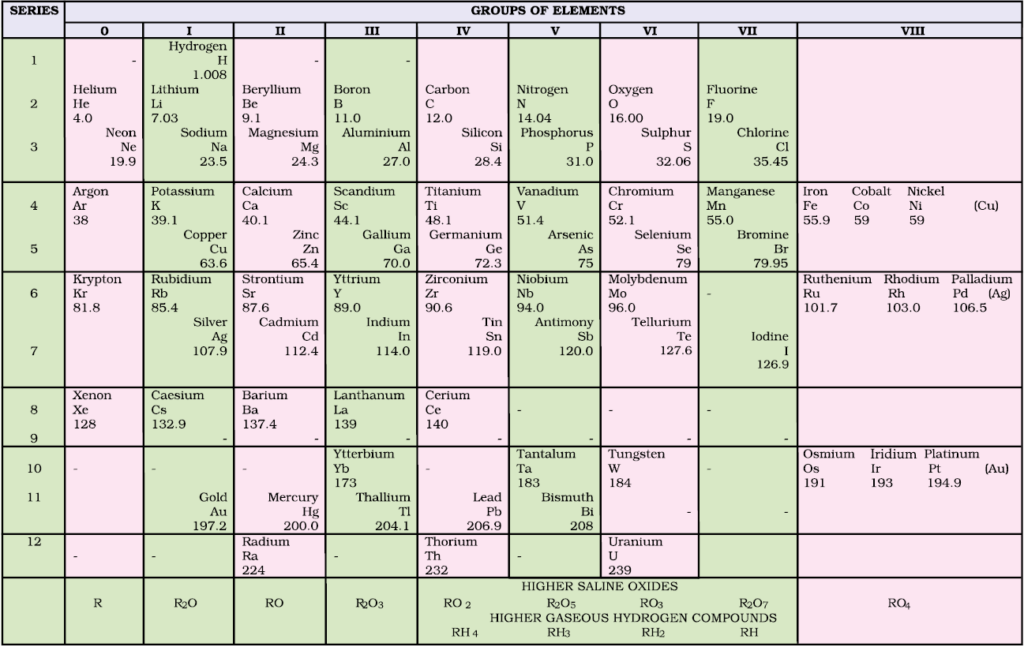
ఆ తర్వాత మోస్లే ఆవర్తన నియమాన్ని అభివృద్ధి చేశాడు. మెండలీవు చెప్పిన “పరమాణుభారాల ఆవర్తన ప్రమేయాలు” అనేదాన్ని మార్చి “పరమాణు సంఖ్యల ఆవర్తన ప్రమేయాలు” అని ఆవర్తన నియమాన్ని నిర్వచించాడు. ఫలితంగా మూలకాల వర్గీకరణ మెండలీవ్ వర్గీకరణ కంటే మరింత స్పష్టంగా చక్కగా వర్గీకరణం చేయడం సాధ్యమైంది.
తర్వాత ఆధునిక పరమాణు నిర్మాణాన్ని శాస్త్రవేత్తలు ఆవిష్కరించారు. అందులో ముఖ్యమైనది క్వాంటం సిద్ధాంతం, క్వాంటం నెంబర్లు.
పరమాణువుల్లో ఎలక్ట్రాన్లు అమరి తిరుగుతుండే విధానాన్ని అంటే ఎలక్ట్రాన్ విన్యాసాన్ని కనుగొన్నారు.
మూలకాల ఎలక్ట్రాన్ విన్యాసాలే మూలకాల భౌతిక రసాయన ధర్మాలను నిర్ణయిస్తాయని రూఢీ అయింది. అందుకని ఇప్పుడు ఆవర్తన నియమాన్ని ఇలా చెప్పవచ్చు “మూలకాల భౌతిక రసాయన ధర్మాలు ఎలక్ట్రాన్ విన్యాసాల ఆవర్తన ప్రమేయాలు”.
ఇంకా చెప్పాలంటే “మూలకాల భౌతిక రసాయన ధర్మాలు వ్యాలెన్సీ ఎలక్ట్రాన్” (చిట్టచివరి కర్పరం లోని చివరి ఆర్బిటాల్ లోని ఎలక్ట్రాన్) విన్యాసపు ఆవర్తన ప్రమేయాలుగా అర్థం చేసుకోవచ్చు.
ఏ మూలకాల చిట్ట చివరి ఆర్బిటాల్ S అయి ఉండి ఎలక్ట్రాన్లు నిండుతూ ఉంటే వాటిని “S” బ్లాకు మూలకాలు అంటారు. S ఆర్బిటాల్ లో రెండు ఎలక్ట్రాన్లు మాత్రమే నిండే అవకాశం ఉంది కనుక S బ్లాక్ మూలకాలు రెండు గ్రూపులు గా అంటే 1A, 2A గ్రూపులుగా ఉంటాయి.
ఏ మూలక పరమాణువుల్లో చివరి “P” ఆర్బిటాల్ల ఎలక్ట్రాన్లు నిండుతూ ఉంటే P గ్రూపు మూలకాలు అంటారు. P ఆర్బిటాల్లో 6 ఎలక్ట్రాన్లు నిండి అవకాశం ఉంది కనుక P బ్లాక్ మూలకాలు ఆరు గ్రూపులుగా ఉంటాయి అవి lllB, IVB, VB, VIB, VIIB, 0 గ్రూపు మూలకాలు అని అంటారు.
పీరియాడిక్ టేబుల్ లో “S” బ్లాక్ ఎడమవైపున, “P” బ్లాక్ కుడివైపున ఉంటాయి. ఈ రెండు బ్లాక్ మూలకాలని ప్రాతినిధ్య మూలకాలు అని కూడా అంటారు. ఈ రెండు బ్లాక్ ల మూలకాల మధ్య “D” బ్లాక్ మూలలు ఉన్నాయి. D బ్లాక్ మూలకాల్లో D ఆర్బిటాల్లలో ఎలక్ట్రాన్లు నిండుతూ వస్తాయి. “F” ఆర్బిటాల్ లో ఎలక్ట్రాన్లు నిండుతూ వస్తే వాటిని “F” బ్లాక్ మూలకాలు అంటారు. లేదా అంతర పరివర్తన మూలకాలు అని కూడా అంటారు.
ఏ గ్రూపులోనైనా ఒక మూలకపు ధర్మం తెలిసి ఉంటే మిగిలిన మూలకాల ధర్మాలు కూడా ఇంచుమించు అదే విధంగా ఉంటాయి. అందుకని కొన్ని మూలకాలు అధ్యయనం చేస్తే ఆ మిగిలిన ఆ గ్రూపులో మిగిలిన మూలకాలన్నట్లు గురించి అవగాహన వస్తుంది
పిరియాడిక్ టేబుల్ లో అడ్డు వరుసలు ఏడు ఉన్నాయి. వీటిని పీరియడ్లు అంటారు. ఒక్కొక్క వరుస క్వాంటం సంఖ్యను సూచిస్తుంది. మొదటి వరుసలో రెండు మూలకాలే ఉంటాయి. అంటే ఆ కర్పరంలో రెండు ఎలక్ట్రాన్లు మాత్రమే నిండి ఉండే అవకాశం ఉంది గనుక రెండవ పీరియడ్లో 8 ఎలక్ట్రాన్ లు నిండే అవకాశం ఉంది కనుక దీనిలో 8 మూలకాలు ఉంటాయి. మూడో వరుసలో కూడా 8 ఎలక్ట్రాన్లు నిండే అవకాశం ఉంది కనుక ఈ పీరియడ్ లో 8 మూలకాలే ఉంటాయి. నాలుగో వరుసలో అంటే పీరియడ్లో అట్లాగే ఐదో పీరియడ్లో 18 ఎలక్ట్రాన్ లో నిండే అవకాశం ఉంది కనుక ఈ పీరియడ్లలో 18 మూలకాలు ఉంటాయి. అలాగే ఆరవ పీరియడ్లో ఏడవ పీరియడ్లో 32 ఎలక్ట్రాన్లు నిండి అవకాశం ఉంటుంది. అయితే 6వ పీరియడ్లో లాంతీనియం తర్వాత 14 మూలకాలను వేరుచేసి క్రింద అమర్చారు వీటిని లాంతనైడ్లు అంటారు. 7 ఏడవ పీరియడ్ లో కూడా ఆక్టీనియం తర్వాత 14 మూలకాలను కూడా కింద అమర్చారు . వీటిని యాక్టినైడ్లు అంటారు. ఈ యాక్టినైడ్లు లాంథనైడ్లు లో “F” బ్లాకు మూలకాలు అంటే “F” ఆర్బిటాల్ లో ఎలక్ట్రాన్లు నిండుతాయి. కనుక ఈ రెండు మూలకాలనీ ప్రత్యేకంగా పీరియాడిక్ టేబుల్ లో కింద చేర్చారు. ఇప్పుడు దీన్ని విస్తృత ఆవర్తన పట్టిక (long form of the periodic table) అంటారు.
మూలకాల భౌతిక రసాయన ధర్మాలు పరమాణువులోని చిట్టచివరి కర్పరం(shell) లోని చివరి ఆర్బిటాల్ లోని ఎలక్ట్రాన్ విన్యాసాన్నిబట్టి ఉంటాయి.

పిరియాడిక్ టేబుల్ ని గమనిస్తే ప్రతి మూలకం యొక్క పరమాణు భారం పరమాణు సంఖ్య ఎలక్ట్రాన్ విన్యాసం తెలుస్తుంది. కనుక ఆ మూలకాల ధర్మాలు కూడా అర్థమవుతాయి. పైగా గ్రూపులోని ఒక మూలకం గురించి తెలుసుకుంటే మిగిలిన మూలకాలు కూడా ఇంచుమించుగా అవగాహనకు వస్తాయి. ఆ విధంగా 118 మూలకాలను సులభంగా అర్థం చేసుకొని గుర్తుపెట్టుకొని అవకాశం ఉంది. మొత్తం రసాయన శాస్త్ర సారాన్ని ఒక్క పేజీలో ఇమిడి ఉండే పీరియాడిక్ టేబుల్ ద్వారా మనం అర్థం చేసుకోవచ్చు.
ఇంత మంచి జ్ఞాన నిధిని తెలుసుకునేందుకు
పదో తరగతి స్థాయిలోపు విద్యార్థులకు లేకపోవడం వారికి నష్టమే.
M.V. Chalapathi, Nellore
9490300906

Periodic Table గురించి ప్రతి ఒక్క విద్యార్థి తప్పకుండా తెలుసుకోవాలి. మంచి సమాచారం పోస్ట్ చేశారు… JVV వారు.. వారికి వారి రచయితల టీమ్ కు అభనందనలు.